Editora: Lisiane Martins.
Colaboradores: Amanda Lewandowski da Silva, Giovani Meneguzzi de Carvalho, João Francisco Petry, Mariana da Silva Ribeiro e Pâmella Caroline Kreling.
DOPAMINA[]
A dopamina está envolvida em vários distúrbios da função cerebral, como doença de Parkinson, Esquizofrenia, déficit de atenção e distúrbios endócrinos. Sua distribuição no cérebro é mais restrita que a da noradrenalina. Uma grande porção do seu conteúdo no cérebro é encontrada no corpo estriado (uma parte do sistema motor extrapiramidal relacionada com a coordenação do movimento) e existe também uma alta concentração em certas partes do sistema límbico e no hipotálamo.
· Via nigroestriatal: importante no controle motor;
· Vias mesolímbica/mesocortical: envolvidas na emoção e em sistemas de recompensa induzidos por drogas;
· Neurônios túbero-hipofisários: se estendem do hipotálamo até a hipófise, cujas secreções regulam.
A síntese de dopamina segue a mesma via que a noradrenalina, que consiste na conversão da tirosina em DOPA (etapa que limita a velocidade do processo), seguida de descarboxilação para formar dopamina. Depois de liberada e de ter atuado nos receptores, é retirada da fenda sináptica por transportadores proteicos (co-transportadores de dopamina e sódio) para o interior do terminal axonal pré-sináptico, onde a dopamina será armazenada em vesículas novamente, e o excesso degradado por ação enzimática. A dopamina é metabolizada pela MAO e COMT, sendo os produtos principais: ácido diidroxifenilacético (DOPAC) e o ácido homovanílico (HVA), que são excretados na urina. Os produtos finais são conjugados de sulfato, envolvendo a ação da enzima sulfotransferase.
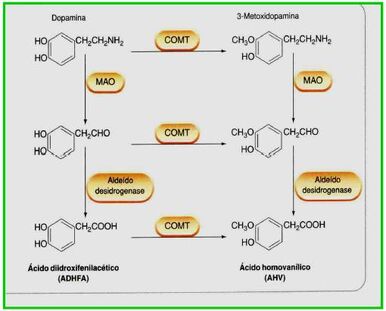
Metabolização da Dopamina - Fonte: Daniela Delwing de Lima, 2013 (apresentação ppt feita em sala)
Receptores de Dopamina:[]
São receptores transmembrana acoplados à proteína G (tipo 2). Existem dois tipos de receptores, D1 e D2. Estão associados, respectivamente, à ativação e inibição da adenilato ciclase (levando ou não à formação de AMPc). A família original de receptores D1 inclui atualmente D1 e D5, enquanto a família D2 (farmacologicamente mais importante no SNC) é constituída de D2, D3 e D4.
Receptores D1: Mais abundantes e disseminados em áreas que recebem inervação dopaminérgica (estriado, sistema límbico, tálamo e hipotálamo). Também medeiam diversos efeitos na periferia, principalmente vasodilatação renal (devido ao aumento do AMPc) e aumento da contratilidade do miocárdio (por aumentar a concentração intracelular de cálcio).
Receptores D2: Da mesma maneira que os receptores D1 estão no estriado, sistema límbico, tálamo, hipotálamo e, neste caso, também se encontram na hipófise. Os receptores de dopamina importantes para a ações dos agentes antipsicóticos pertencem principalmente à família destes receptores. Na hipófise anterior, causam inibição da secreção de prolactina. Desencadeamento do vômito.
Receptores D3: Encontrados no sistema límbico, mas não no estriado. Os receptores D3 pré-sinápticos são encontrados principalmente em neurônios dopaminérgicos, por exemplo, os situados no sistema estriado e límbico, onde atuam ao inibir a síntese e a liberação de dopamina (autorreceptor).
Receptores D4: Muito mais fracamente expresso, principalmente no córtex e no sistema límbico, porém é alvo de interesse em virtude de sua possível relação com o mecanismo da esquizofrenia e dependência de drogas. No córtex, é importante pelo controle da alerta e do humor. Apresenta acentuado polimorfismo no ser humano.
Funções da Dopamina:[]
· Controle motor (sistema nigroestriatal);
· Efeitos comportamentais (sistemas mesolímbico e mesocortical);
· Controle endócrino (sistema túbero-hipofisário).
A doença de Parkinson é um distúrbio no controle motor, associado a uma deficiência de dopamina na via nigroestriatal.
Muitos agentes psicóticos são antagonistas dos receptores D2, cujo efeito colateral principal consiste em causar distúrbios do movimento.
Efeitos Comportamentais:[]
Os efeitos comportamentais da atividade da dopamina em excesso consistem em padrões comportamentais estereotipados, que podem ser produzidos por agentes liberadores (como a anfetamina) e agonistas (como a apomorfina) da dopamina.
Existem algumas evidências de que a esquizofrenia no ser humano está associada a uma hiperatividade dopaminérgica. Em ratos, a administração de anfetamina produz vários tipos de interação social anormal, incluindo comportamento isolado e agressivo. Todavia, é difícil quantificar esses efeitos ou estabelecer relação com a esquizofrenia no homem.
Função Neuroendócrina:[]
A via dopaminérgica túbero-hipofisária está envolvida no controle da secreção de prolactina. A dopamina é um dos diversos mediadores secretados pelo hipotálamo (que controlam a secreção de diversos hormônios da hipófise) que exerce efeito inibitório sobre a liberação de prolactina. Muitos agentes antipsicóticos, através do bloqueio de receptores D2, aumentam a secreção de prolactina, podendo induzir o desenvolvimento da mama e a lactação, até mesmo no sexo masculino.
Em indivíduos normais, a dopamina produz aumento do hormônio do crescimento.
Vômitos:[]
Evidências farmacológicas sugerem fortemente que os neurônios dopaminérgicos têm alguma atividade na produção de náuseas e vômitos. Por conseguinte, quase todos os agonistas dos receptores de dopamina e outras drogas que aumentam a liberação de dopamina no cérebro causam náusea e vômitos como efeitos colaterais, ao passo que muitos antagonistas da dopamina possuem atividade antiemética. Ocorrem receptores D2 na área do bulbo (zona de gatilho quimiorreceptora) associados ao desencadeamento do vômito.
SEROTONINA – 5-HIDROXITRIPTAMINA (5-HT)[]
Embora o cérebro seja responsável por apenas 1% do conteúdo corporal total de 5-HT, trata-se de um importante transmissor do SNC. A 5-HT assemelha-se à adrenalina em sua síntese, armazenamento e liberação. Seu precursor é o triptofano, um aminoácido derivado da proteína dietética, que não é produzido pelo nosso organismo e cujo nível plasmático varia consideravelmente de acordo com a ingestão de alimentos (carnes, grãos, laticínios) e o momento do dia. Uma dieta pobre em triptofano leva à redução da serotonina.
O triptofano é ativamente captado pelos neurônios, convertido pela triptofano hidroxilase em 5-hidroxi-triptofano e, a seguir, descarboxilado por uma aminoácido descarboxilase inespecífica em 5-HT. Acredita-se que a disponibilidade de triptofano (principalmente) e a atividade da triptofano hidroxilase constituem os principais processos que regulam a síntese de 5-HT.
Após a sua liberação, a 5-HT é, em grande parte, recuperada por captação neuronal, sendo este mecanismo inibido por muitas das mesmas drogas que inibem a captação de catecolaminas, como os antidepressivos tricíclicos, por exemplo. Os inibidores específicos da recaptação da serotonina constituem um importante grupo de agentes antidepressivos. A 5-HT é degradada quase totalmente pela MAO, que a converte em 5-hidroxiindol acetaldeído, cuja maior parte é desidrogenada para formar o ácido 5-hidroxiindolacético, que é excretado na urina. Essa excreção urinária fornece uma medida de renovação da 5-HT. Além disso, os transportadores proteicos (co-transportadores de sódio) relacionados à finalização da ação da serotonina são alvo da ação de fármacos (como a fluoxetina, por exemplo – inibidor seletivo da recaptura de serotonina).
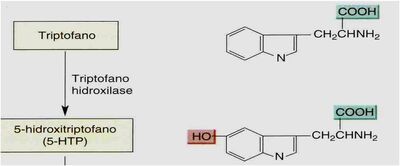
Triptofano Hidroxilase - Fonte: Daniela Delwing de Lima, 2013 (apresentação ppt feita em sala).

5-HTP Descarboxilase - Fonte: Daniela Delwing de Lima, 2013 (apresentação ppt feita em sala).
Vias da 5-HT no SNC:[]
A distribuição dos neurônios que contêm 5-HT é muito disseminada e assemelha-se à dos neurônios noradrenérgicos. As células formam vários grupamentos grandes na ponte e na porção superior do bulbo, que se situam próximo à linha média (rafe) e são frequentemente denominados núcleos da rafe.
===Receptores de 5-HT no SNC: ===
Todos consistem em receptores acoplados à proteína G (receptores tipo 2), com exceção do 5-HT3, que é um canal de cátion regulado por ligante (receptor tipo 1). Todos são expressos no SNC, porém a maioria dos dados funcionais cita os três membros mais importantes do grupo: os receptores 5-HT1, 5-HT2 e 5-HT3.
5-HT1: Predominantemente inibitórios nos seus efeitos (autorreguladores).
5-HT1A: expressos como autorreceptores pelos neurônios de 5-HT, com efeito auto-inibitório. Estão amplamente distribuídos no córtex e na amígdala, e acredita-se que constituam o principal alvo de drogas utilizadas no tratamento da ansiedade e depressão. Também está relacionado com efeitos comportamentais (sono, alimentação, termorregulação, ansiedade).
5-HT1B e 5-HTD são encontrados principalmente como receptores inibitórios pré-sinápticos nos gânglios da base.
5-HT2: Exercem um efeito pós-sináptico excitatório e aparecem em abundância no córtex e no hipocampo (principalmente 5-HT2A). Acredita-se que constituam o alvo de várias drogas alucinógenas. O uso de antagonistas dos receptores 5-HT2 é feito na enxaqueca.
5-HT3 - ionotrópico: Encontrados principalmente na área postrema (região do bulbo envolvida com o vômito) e em outras partes do tronco cerebral, estendendo-se até o corpo dorsal da medula espinhal. São também amplamente encontrados, de forma mais dispersa, em certas partes do córtex e SNP. Estão relacionados com excitação neuronal (autônoma, neurônios nociceptivos) e êmese (vômito), além de efeitos comportamentais como a ansiedade. Como é receptor do tipo 1, a serotonina atuando nele tem efeito excitatório e rápido.
5-HT4: Aumento da motilidade gastrointestinal, excitação neuronal, e efeito facilitador pré-sináptico (estimulando liberação de acetilcolina). Assim, a serotonina nesse receptor tem papel cognitivo (aprendizado, memória) por estimular a liberação de Ach.
5-HT5: Pouco se sabe acerca da sua função e farmacologia.
5-HT6: Presente apenas no SNC (córtex, hipocampo e sistema límbico), sendo alvo para fármacos que servem para melhorar a função cognitiva.
5-HT7: No córtex, hipocampo, tálamo, hipotálamo. Age nos vasos sanguíneos, no TGI, na termorregulação, regulação endócrina, humor, função cognitiva e sono. Uma diminuição da serotonina pode estar associada ao aumento do cortisol, gerando depressão.
Aspectos Funcionais:[]
· Alucinações (LSD-alucinógeno) e alterações comportamentais;
· Comportamento de alimentação;
· Controle do humor e da emoção;
· Controle do sono/vigília;
· Controle das vias sensoriais, incluindo nocicepção (efeito inibitório sobre a transmissão na via da dor, verificando-se efeito sinérgico entre 5-HT e analgésicos como a morfina);
· Controle da temperatura corporal, pressão arterial e função sexual;
· Vômito.
(Quanto menos serotonina: mais sono, mais fome, mais dor, mais frio, menos atividade sexual).
GLUTAMATO[]
Faz parte dos principais neurotransmissores rápidos no SNC, que consistem no transmissor excitatório glutamato, e nos transmissores inibitórios GABA e glicina, (estes últimos serão abordados num próximo momento).
O L-glutamato é o principal transmissor excitatório ubíquo no SNC. Tem distribuição ampla e bastante uniforme, com importante função metabólica. Nos neurônios do SNC, ele provém principalmente da glicose, através do ciclo de Krebs, ou da glutamina, que é sintetizada por células gliais e captada pelos neurônios.
Do mesmo modo que ocorre com outros transmissores, o glutamato é armazenado em vesículas sinápticas e liberado por exocitose cálcio-dependente. Existem proteínas transportadoras específicas (movidas por gradiente de prótons) responsáveis pela sua captação por neurônios e outras células e pelo seu acúmulo nas vesículas sinápticas (por antiporte – entra glutamato e sai prótons). Ao contrário do que foi observado na síntese e no transporte das monoaminas, existem poucas drogas conhecidas (e nenhuma em uso clínico) que interferem de forma específica no metabolismo do glutamato.
A ação do glutamato é interrompida principalmente pela sua recaptação, mediada por transportador dependente de sódio nas terminações nervosas e nas células vizinhas da glia. Em processos patológicos como na isquemia cerebral, o transporte pode ocorrer de modo inverso, de forma que haja liberação de mais glutamato (ao invés de interromper a ação). Isso acontece, por exemplo, devido à despolarização por aumento do potássio extracelular.

Síntese e Finalização da Ação do Glutamato - Fonte: Daniela Delwing de Lima, 2013 (apresentação ppt feita em sala)
Receptores de Glutamato:[]
Os receptores de glutamato são mais abundantes no córtex, nos gânglios da base e nas vias sensoriais. São classificados de acordo com seus agonistas, e existem quatro subtipos principais de receptores de aminoácidos excitatórios:
· Receptores de NMDA;
· AMPA;
· Cainato;
· Metabotrópicos.
Os três primeiros são geralmente denominados receptores ionotrópicos, e consistem em canais iônicos regulados por ligantes. Os receptores NMDA e AMPA exibem uma co-ligação, enquanto os receptores de cainato exibem uma distribuição muito mais restrita.
Receptores NMDA:
São formados a partir de dois tipos de subunidades, NR1 e NR2.
Aspectos especiais desses receptores:
· São altamente permeáveis ao sódio e cálcio;
· São rapidamente bloqueados por íons de Mg⁺⁺ (dependente de voltagem);
· Determinados anestésicos e agentes psicomiméticos são bloqueadores seletivos dos canais. Ex: cetamina e fenciclidina;
· São passíveis de facilitação por moduladores que atuam em sítios distindos do sítio de ligação do glutamato. A abertura do canal requer tanto glicina, quanto glutamato (o sítio de ligação para a glicina (D-serina) é distinto do sítio de ligação do glutamato, e ambos precisam estar ocupados). Existem antagonistas competitivos que bloqueiam essa ação da glicina e, portanto, inibem indiretamente a ação do glutamato.
Receptores de AMPA:[]
GluR1-4 e ausência de GluR2 (isso os torna mais permeáveis a cálcio do que os demais). É permeável a sódio. Receptores cainato:
GluR5-7 com KA1,2. Permeável a sódio e pouco permeável a cálcio.
Receptores Metabotrópicos:[]
Estão acoplados às proteínas G, ligados a sistemas de segundos mensageiros intracelulares, tendo sido também detectados subtipos múltiplos (em número de oito até agora):
Grupo I: mGLU1 e mGLU5: ativa proteína Gq (formando IP3)
Grupo II: mGLU2 e mGLU3: ativa proteína Gi (inibe adenilato ciclase)
Grupo III: mGLU4, mGLU6, mGLU7 e mGLU8: ativa proteína Gi (inibe adenilato ciclase)
São peculiares por dois motivos: não exibem nenhuma homologia de sequência com outros receptores acoplados à proteína G e possuem uma grande cauda N-terminal extracelular que cotem o sítio do glutamato (ao contrário da maioria dos receptores de amina, em que o sítio de ligação de agonistas fica mergulhado entre as hélices transmembrana).
Funções dos Receptores de Glutamato:
NMDA: Esses receptores frequentemente coexistem com os receptores AMPA. Contribuem com um componente lento para o potencial sináptico excitatório pós-sináptico.
AMPA: Transmissão sináptica excitatória rápida no SNC – astrócitos e neurônios.
Cainato: Transmissão excitatória rápida em certas regiões do cérebro (por terem uma distribuição mais restrita).
Metabotrópicos: Ligados à produção de IP3 e liberação de Ca⁺⁺ intracelular ou à inibição da adenilato ciclase. Possuem localização pré e pós-sináptica, e são também encontrados em células não neuronais. Seus efeitos sobre a modulação são mais moduladores do que diretos, consistindo principalmente em efeitos excitatórios pós-sinápticos (através da inibição dos canais de potássio) e em inibição pré-sináptica (através da inibição dos canais de cálcio).
Tanto NMDA quanto os metabotrópicos atuam na plasticidade sináptica, excitotoxidade (porque a entrada de quantidades excessivas de Ca⁺⁺ produzida pela ativação do receptor NMDA pode resultar em morte celular pelo excesso de atividade) e patogenia da epilepsia.
Antagonistas do Glutamato:[]
Ainda não foram desenvolvidos antagonistas dos receptores de aminoácidos excitatórios para uso clínico. O interesse terapêutico potencial reside, principalmente, na redução da lesão cerebral após acidentes vasculares cerebrais e lesão encefálica, no tratamento da epilepsia e para várias outras indicações como a esquizofrenia. Os estudos realizados até agora trazem desvantagens como tendências a distúrbios alucinatórios, depressão global do SNC, além de pequena margem de segurança.
REFERÊNCIAS[]
- FUCHS, Flávio Danni; WANNMACHER, Lenita. Farmacologia Clínica: fundamentos da terapêutica racional. 4. ed. Rio de Janeiro: Guanabara Koogan, 2010.
- MARTINS, Lisiane. Anotação da aula da Disciplina de Farmacologia. UNIVILLE. 12/06/2013.
- RANG, H. P.; DALE, M. M. Rang & Dale. Farmacologia. 7. ed. Rio de Janeiro: Elsevier, 2011.